Am 18. Oktober hat die Food and Drug Administration (FDA) das zweite genverändernde Krebstherapeutikum für Patienten mit diffusem großem B-Zell-Lymphom (DLBCL), der häufigsten aggressiven Form des Non-Hodgkin-Lymphoms (NHL), einem Blutkrebs, zugelassen. Die neue Therapie, Yescarta, ist nur für Erwachsene zugelassen, die zwei oder mehr gescheiterte Chemotherapien hinter sich haben.
Yescarta, hergestellt von der biopharmazeutischen Firma Kite, ist eine Art Gentherapie. Sie funktioniert, indem sie das eigene Immunsystem eines Patienten umgestaltet und seine eigenen Zellen in ein „lebendes Medikament“ verwandelt, das Krebszellen identifizieren und abtöten kann. Dies ist eine Art der Immuntherapie, die medizinische und genetische Techniken kombiniert, um das Immunsystem der Patienten zur Abwehr von Krankheiten auszustatten. In bestimmten Fällen haben diese Therapien zu erheblichen Remissionen und sogar Heilungen geführt.
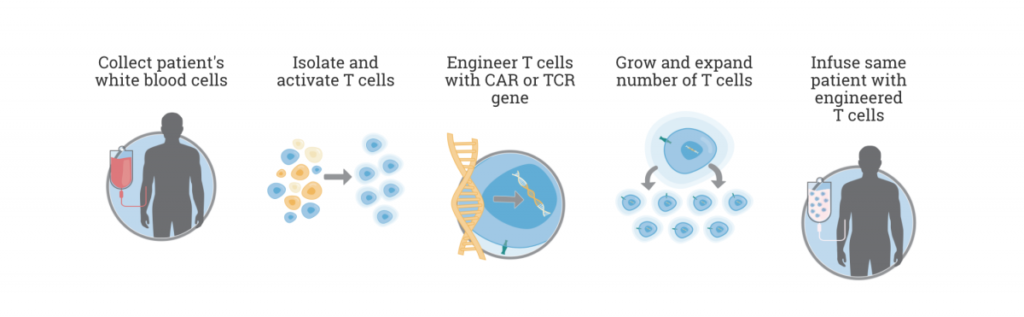
Imun-Gentherapie von Kite Pharma
„Heute ist ein wichtiger Tag für Patienten mit rezidiviertem oder refraktärem B-Zell-Lymphom, die aus Optionen heraus gelaufen sind und auf neue Behandlungen gewartet haben, die ihnen in ihrem Kampf gegen Krebs helfen können,„sagte der CEO John Milligan von Gilead Sciences in einer Pressemitteilung (Gilead besitzt Kite ab 2016).
Nichts zu verlieren
Drei von fünf Fällen aggressiver NHL sind die DLBCL-Variante. In den USA gibt es jährlich etwa 7500 Patienten mit refraktärem DLBCL, die für eine CAR T-Therapie in Frage kommen. Nur sieben Prozent der Patienten mit einem refraktären großen B-Zell-Lymphom, die den aktuellen Standard der Behandlung erhalten, erreichen eine vollständige Ansprache, und als Gruppe haben die Patienten typischerweise ein medianes Gesamtüberleben von etwa sechs Monaten. Derzeit fast die Hälfte der Patienten mit großen B-Zell-Lymphom, die überleben, um die zweite oder spätere Linien der Therapie zu unternehmen, nicht auf die Behandlung ansprechen und schnell Rückfallen.
Ungefähr 3500 Amerikaner jedes Jahr konnten Anwärter für Yescarta, eine einmalige intravenöse Infusion sein, die individuell für jeden Patienten 373.000 $ in der Herstellung kostet. Die Behandlung ist riskant und kann mit lebensbedrohlichen Nebenwirkungen wie neurologischen Problemen, schweren Infektionen und sogar dem Tod einhergehen. Da die berechtigten Patienten jedoch ein so hohes Sterberisiko haben, scheinen die meisten der Meinung zu sein, dass es das Risiko wert ist.
Tina Bureau, ein Lymphom-Patientin, die an der Studie des Medikaments teilgenommen hat und sich jetzt in Remission befindet, erzählte der New York Times keine andere Behandlung, bis Yescarta für sie arbeitete. „Ja, das kann lebensbedrohliche Probleme bereiten„, sagte das FBI. „Aber wenn du in einer Situation bist, in der dein Leben sowieso bedroht ist, habe ich nicht das Gefühl, dass Du etwas zu verlieren hast.“